Pengertian Atom Rutherford, Kelebihan dan Kekurangannya – Pada kesempatan ini Seputar Pengetahuan akan membahas tentang Atom Rutherford. Yang mana dalam pembahasan kali ini menjelaskan pengertian atom rutherford, teori, kelebihan dan kekurangannya dengan secara singkat dan jelas. Untuk lebih jelasnya simak artikel berikut ini.
Pengertian Atom Rutherford, Kelebihan dan Kekurangannya
Elektron-elektron pada sebuah atom ini bisa terikat pada inti atom oleh gaya elektromagnetik. Dari beberapa sekumpulan atom demikian juga bisa berhubungan satu sama lainnya, serta juga dapat membentuk sebuah molekul.
Atom yang mengandung jumlah proton serta elektron yang sama memiliki sifat netral,lalu sedangkan yang mengandung jumlah proton atau juga elektron yang berbeda bersifat positif atau juga negatif sering disebut ialah sebagai ion.
Atom ini juga dikelompokkan dengan berdasarkan jumlah proton serta neutron yang terdapat pada inti atom tersebut. Jumlah proton pada atom tersebut akan menentukan unsur kimia atom tersebut, serta jumlah neutron menentukan isotop unsur tertentu.
Pengertian Atom
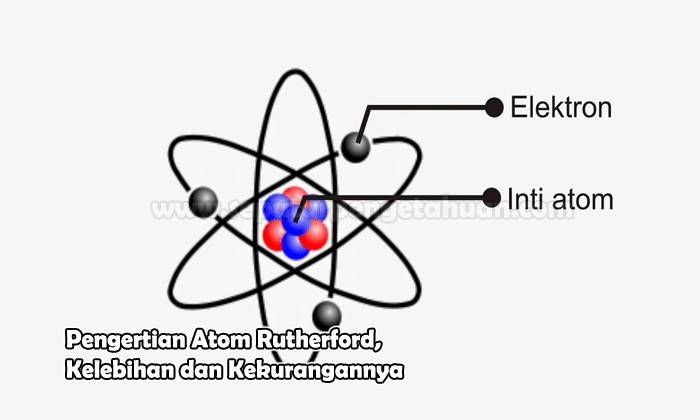
Atom ini merupakan suatu satuan dasar materi, yang terdiri dari inti atom dan juga awan elektron yang bermuatan negatif yang akan mengelilinginya. Inti atom ini terdiri dari proton yang bermuatan positif, atau juga neutron memiliki muatan netral.
Dasar Teori Atom Ernerst Rutherford
Setelah Teori Atom Jhon Dalton itu disangkal serta juga kemudian diperbaiki oleh Jj. Thomson ini menyatakan bahwa atom tersebut seperti Roti Kismis. Selanjutnya giliran Rutherford yang bisa menyangkal kebenaran teori atom Thomsom.
Di kala itu Rutherford mengatakan bahwa atom tersebut mempunyai sebuah inti pusat atau sering disebut nekleus dengan dikelilingi awan elektron memiliki muatan negatif.
Teori atom Rutherford tersebut didasarkan pada eksperimen penembakan inti atom lempengan emas pada partikel alfa yang sering dikenal dengan sebutan percobaan Geiger-Marsden. di waktu itu, Rutherford tersebut akan menyusun desain rancangan percobaan penembakan atom emas oleh partikel alfa yang sudah dipancarkan oleh unsur radio aktif.
Ternyata, sinar radio aktif tersebut ada yang telah dipantulkan, dibelokkan, atau juga diteruskan. Rutherford tersebut lalu menjelaskan bahwa apabila partikel alfa tersebut mengenai inti atom. Maka akan terjadi tumbukan yang menyebabkan pembelokan atau pemantulan partikel alfa. Hal ini disebabkan oleh karena massa serta muatan atom yang terpusat pada inti nukleus.
Rutherford tersebut lalu menyarankan bahwa muatan inti atom akan sebanding dengan massa atom di dalam SMA/satuan masa atom. Partikel alfa yang mengenai awan elektron tersebut tidak akan dibelokkan atau dipantulkan.
Dari hasil pemahamannya dengan melaui eksperimennya tersebut, Ernerst Rutherford tersebut akhirnya menyimpulkan yang menyatakan bahwa:
- Sebagian besar volume atom itu merupakan ruang hampa.
- Massa atom akan terpusat pada inti atom (nukleus).
- Muatan atom tersebut dapat terkonsentrasi pada pusat atom dengan volume yang lumayan kecil.
- Kelipatan muatan itu sebanding dengan massa atom.
Dengan melalui pernyataannya E. Rutherford ini bisa menyangkal bahwa atom itu bukanlah seperti roti kismis. Melainkan seperti susunan planet yang mengorbit matahari. Di mana matahari tersebut akan diumpamakan sebagai inti pusat yang bermuatan positif (nukleus) atau susunan planet yang diumpakannya sebagai muatan negatif.
Oleh karena itu, teori atom Dalton serta Thomson yang memiliki kelebihan ataupun kelemahannya. Teori atom E. Rutherford ini mempunyai kelebihan dan kelemahannya. Dibawah ini merupakan kelebihan serta kelemahan dari teori atom E. Rutherford.
Kelebihan dan Kekurangan Teori Atom Ernerst Rutherford.
Adapun Kelebihan dan Kekurangan Teori atom ernerst rutherford ini ialah sebagai berikut :
Kelebihan Teori Atom Ernerst Rutherford
- Mudah dipahami untuk dapat menjelaskan struktur atom yang sangat rumit.
- Dapat menjelaskan bentuk dari suatu lintasan elektron yang mengelilingi inti atom.
- Bisa menggambarkan gerak elektron disekitar inti.
Kekurangan Teori Atom Ernerst Rutherford
- Model atom rutherford ini belum mampu untuk menjelaskan dimana letak elektron serta juga cara rotasinya terhadap ini atom.
- Elektron ini dapat memancarkan energi pada saat bergerak,lalu sehingga energi atom menjadi tidak stabil.
- Tidak bisa menjelaskan spektrum garis pada atom hidrogen (H).
Demikian penjelasan tentang Pengertian Atom Rutherford, Kelebihan dan Kekurangannya. Semoga dapat bermanfaat dan menambah wawasan Anda. Terima kasih.
Daftar Isi
